اطلاعات کامل عناصر و کاملترین جدول تناوبی
اطلاعاتی از جمله خواص مهم عناصر و حالت و شکلهای اوربیتالی و ایزوتوپ های عناصر با کلیک بر روی لینک زیر:
دیگر امکانات آنلاین در ادامه مطلب

اطلاعات کامل عناصر و کاملترین جدول تناوبی
اطلاعاتی از جمله خواص مهم عناصر و حالت و شکلهای اوربیتالی و ایزوتوپ های عناصر با کلیک بر روی لینک زیر:
دیگر امکانات آنلاین در ادامه مطلب
جدول مندلیف در تنظیم و پایدار کردن جرم اتمی بسیاری از موارد مندلیفنادرست بودن جرم اتمی برخی از عناصر را ثابت و برخی دیگر را درست کرد .


اینم یه روش خوب برای حفظ کردن جدول تناوبی:
گروه۱:لیلا(Li) نكند(Na) كه(k) روبه(Rb) سوزانده(Cs) فرنگیز(Fr).
گروه۲:بگو(Be)منیژه(Mg) كله ات را(Ca) سرویس میكنم (Sr)با(Ba) رنده(Ra).
گروه۳:بگو (B) الو (Al) جواد (Ga) اینجا (In) تیمارستان(Ti).
گروه۴:كسی© (Si) گریه(Ge) نكندسر (Sn) بی پولی(Pb).
گروه۵:نگو (N) پرسپولیس (P) اس آ اس (As) بگواستقلال(Sb) بی طرفه(Bi).
گروه۶:اه(O) سنی(S) سویرم(Se) تلی (Te) پروفسور(Po) .(تركی)
گروه۷:فرید (F) كلم (Cl) برد (Br) ایرج (I) آتش (At).
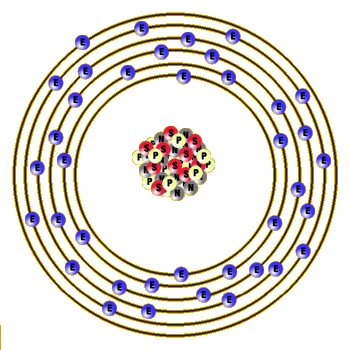
| عدد اتمی که با نماد Z نشان داده میشود، تعداد واحدهای بار مثبت هسته است و چون پروتون بار 1+ دارد، پس عدد اتمی ، تعداد پروتونهای موجود در هسته اتم است. از طرف دیگر ، اتم از لحاظ بار الکتریکی ، خنثی است. بنابراین عدد اتمی ، تعداد الکترونهای خارج از هسته یک اتم ترکیب نشده را نیز نشان میدهد. |
بعضی از گروههای عناصر از لحاظ خواص شیمیایی و فیزیکی بسیار به هم شبیهاند. یکی از این گروهها هلیم (He) ، نئون (Ne) ، آرگون (Ar) ، کریپتون (Kr) ، زنون (Xe) و رادون (Rn) است که همگی گازهایی بیرنگاند و واکنشپذیری کمی دارند. این عناصر ، گازهای نجیب نامیده میشوند و عدد اتمی آنها به ترتیب 2 ، 10 ، 18 ، 36 ، 54 و 86 است.
گروه دیگر عناصر که فلزاتی نرم و بسیار واکنش پذیرند، عبارتند از: لیتیم (Li) ، سدیم (Na) ، پتاسیم (K) ، روبیدیم (Rb) ، سزیم (Cs) و فرانسیم (Fr). اعداد اتمی این عناصر که فلزات قلیایی نامیده می شوند، به ترتیب 3 ، 11 ، 19 ، 37 ، 55 و 87 است.
مقایسه اعداد اتمی عناصر در دو گروه گازهای نجیب و فلزات قلیایی
نشان میدهد که اگر فهرستی از عناصر به ترتیب افزایش عدد اتمی تنظیم شود،
به دنبال هر گاز نجیب ، یک فلز قلیایی قرار میگیرد. از بررسی گروههای
دیگر عناصر ، علاوه بر این دو گروه ، معلوم میشود که وقتی عناصر بنابر
عدد اتمی مرتب است شده باشند، خواص عناصر یک الگوی تکراری را نشان
میدهند.
قانون تناوبی میگوید که هرگاه عناصر به ترتیب افزایش عدد اتمی مورد بررسی
قرار گیرند، شباهتهای خواص عناصر بهطور تناوبی تکرار میشود. جدول
تناوبی بر مبنای این قانون تنظیم شده است. طرح جدول به گونه ای است که
عناصر مشابه باهم گروهبندی شدهاند و خواص عناصر را میتوان از مکانی که
در جدول دارند، پیشگویی کرد.
 |
عناصری که در یک ردیف افقی جدول دیده میشوند، بر روی هم یک دوره
مینامند. دوره اول تنها شامل دو عنصر هیدروژن (Z=1) و هلیم (Z=2) است.
دوره دوم مرکب از 8 عنصر است که از لیتیم (Z=3) به نئون (Z=10) میرسد.
دورههای بعدی بهترتیب شامل 8 ، 18 ، 18 . 32 عنصر است.
عناصری که اعداد اتمی آنها از 58 تا 71 است، در پایین جدول دیده میشوند و آنها را لانتانیدها یا لانتونوئیدها
مینامند. این عناصر متعلقند به دوره ششم (که مرکب از 32 عنصر است) و در
واقع باید در بدنه جدول پس از لانتان (Z=58) آمده باشند. اما برای این کار
باید جدول را بهطور عمودی برید، دو قسمت بریده را از هم جدا کرد و
لانتانیدها را در مکان مناسب خود جاگذاری کرد. این آرایش ، معمول نیست،
زیرا جدول طویل میشود و نسخهبرداری یا چاپ آن مشکل است.
همین نکات درباره عناصری با اعداد اتمی 89 تا 103 ملحوظ میشود. این عناصر را آکتینید یا آکتینوئید
مینامند و در زیر لانتانوئیدها ، در ته جدول تناوبی جای دارند. آنها
متعلق به دوره هفتم هستند و باید پس از آکتینیوم (Z=89) جاگذاری شوند. به
استثنای دوره اول ، هر دوره با یک فلز قلیایی آغاز میشود و با یک گاز نجیب
پایان مییابد. عنصر پیش از گاز نجیب ، در هر دوره کامل (به جز نخستین
دوره) ، یک هالوژن که نافلزی بسیار واکنش پذیر است، جای دارد. این هالوژنها
عبارتند از: فلوئور ، کلر ، برم ، ید و استاتین.
عناصری که در یک ستون عمودی جدول ظاهر میشوند، یک گروه یا خانواده نامیده میشوند. عناصر یک گروه ، خواص شیمیایی مشابهی دارند. سه گروهی که از آنها نام بردیم، گروههای گازهای نجیب
، فلزات قلیایی و هالوژنها هستند. هر گروه ، با عنوان خاص مشخص میشود که
معمولا مرکب از یک عدد رومی است و به دنبال آن ، حرف A یا B میآید. اما
برای مشخص کردن گروهها چند سیستم متداول است.

عنصری است که بهطور کلی جلای خاصی دارد، گرما و الکتریسیته را بهخوبی
هدایت میکند و با کوبش ، بدون شکسته شدن به شکلهای گوناگون در میآید.
اما نافلز ، عنصری است که جلای فلزی ندارد، رسانای ضعیفی برای گرما و
الکتریسیته و در حالت جامد شکننده است. خواص شیمیایی فلزات با نافلزات نیز
تفاوت دارد.
در حدود 80% عناصر شناخته شده ، فلز هستند. خط مورب پلهوار جدول تناوبی ،
مشخص کننده تقسیم تقریبی میان فلزات و نافلزات است. نافلزات در طرف راست
این خط قرار میگیرند، اما این تقسیمبندی ، دقیق و کامل نیست. عناصر
نزدیک به این خط ، گاهی شبه فلزات و نیمه فلزات نامیده میشوند. این عناصر ،
خواصی میان فلزات و نافلزات دارند.
در یک دوره ، گستره ای از خواص متفاوت مشاهده میشود. هر دوره ، به
استثنای دوره اول ، با یک فلز بسیار واکنشپذیر یعنی یک فلز قلیایی آغاز
میشود. خواص عناصر بعدی ، از یک عنصر به عنصر دیگر تغییر میکند. خواص
فلزی کاسته میشود و جای آن را خواص نافلزی میگیرد. هر دوره به جز دوره
اول ، با یک نافلز بسیار واکنشپذیر یعنی یک هالوژن که یک گاز نجیب به
دنبال آن میآید، پایان میپذیرد.
این نرم افزار موبایل که برای اولین بار در وبلاگ تخصصی مهندسی شیمی قرار گرفته است جدول تناوبی عنصرها نام دارد که با تمامی موبایل هایی که فرمت جاوا را پشتیبانی میکنند سازگار است.
تمامی خانه های این جدول شامل توضیحاتی است که با انتخاب کردن آن میتوانید به آنها دسترسی پیدا کنید.این نرم افزار علمی را میتوانید بصورت کاملا رایگان از همینجا دانلود کنید.
این هم نگارشی جدید از نرم افزار کاربردی و تخصصی جدول تناوبی عناصر (جدول مندلیوف) که به صورت جاوا عرضه شده است که می تواند برای کنکوری ها و کسانی که علاقه به یادگیری جدول تناوبی دارند بسیار مفید باشد.
توجه: این نرم افزار بر روی تمامی گوشی هایی که از سیستم عامل جاوا پشتیبانی می کنند، با هر اندازه تصویری اجرا می گردد. که البته همه اندازه های در درون یک فایل فشرده برای دانلود قرار داده شده. شما فایل را دانلود کرده و متناسب با گوشی خود یکی از فایلهای قابل نصب با فرمت جاوا را در گوشی خود نصب کنید.
![]() دانلود در ادامه مطلب
دانلود در ادامه مطلب![]()

دانلود در ادامه مطلب